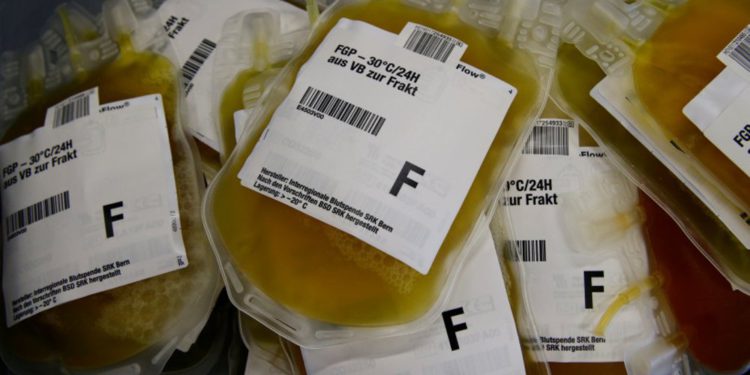
Dos empresas biofarmacéuticas líderes de Israel e Italia continúan su trabajo en el desarrollo y eventualmente la distribución de un tratamiento contra el coronavirus basado en plasma sanguíneo, informaron las empresas en un comunicado el martes.
Las empresas, que son Kamada, con sede en Israel, y Kedrion Biopharma, con sede en Italia, son conocidas por sus terapias derivadas del plasma, y ya han acordado trabajar juntas en su tratamiento contra la COVID-19. Kamada es responsable del desarrollo del producto, así como de su fabricación y presentación a los organismos reguladores, y Kedrion es responsable de la recogida de plasma, que vendrá de los pacientes recuperados del coronavirus, y de la eventual distribución del producto.
Las dos compañías esperan obtener la aprobación de la Administración de Alimentos y Drogas de los Estados Unidos (FDA), así como de otros organismos reguladores en todo el mundo. Ambas compañías también han formado asociaciones con otras instituciones para investigar y probar sus nuevas terapias. En julio, Kedrion se asoció con el Centro Médico Irving de la Universidad de Columbia para probar una nueva terapia de inmunoglobulina (IgG) para los pacientes con coronavirus. El director médico de los laboratorios clínicos del centro, el Dr. Steven Spitalnik, afirmó en ese momento que si recibe la aprobación de la FDA, espera que pueda ser administrada a los trabajadores médicos de primera línea como medida preventiva.
Kamada está actualmente asociado con el Centro Médico de la Universidad de Hadassah, en Jerusalén, donde está probando su tratamiento de IgG bajo los auspicios del Ministerio de Salud.
El tratamiento funciona como una vacuna pasiva, que es cuando se le administran anticuerpos formados por otro paciente que contrajo la enfermedad y los desarrolló. Esto contrasta con una vacuna activa, cuando se le inyecta una versión muerta o debilitada de un virus que engaña a su sistema inmunológico haciéndole creer que ha tenido la enfermedad, y su sistema inmunológico crea anticuerpos para protegerle.
La FDA dio una “autorización de uso de emergencia” para los tratamientos contra el coronavirus que utilizan plasma sanguíneo de pacientes recuperados. El Ministerio de Salud de Israel aún no lo ha hecho, pero el jefe de Hadassah, Zeev Rotstein, les insta a seguir los pasos de la FDA.
“Desde el primer momento en que la COVID-19 atacó a Israel nos dimos cuenta de que el plasma era una herramienta importante para tratar a los pacientes enfermos”, señaló Rotstein al Jerusalén Post.
“El Ministerio de Salud se mostró reacio incluso a vernos recoger el plasma. Pero al final, los frutos son muy satisfactorios”.
Las empresas, que son Kamada, con sede en Israel, y Kedrion Biopharma, con sede en Italia, son conocidas por sus terapias derivadas del plasma, y ya han acordado trabajar juntas en su tratamiento contra la COVID-19. Kamada es responsable del desarrollo del producto, así como de su fabricación y presentación a los organismos reguladores, y Kedrion es responsable de la recogida de plasma, que vendrá de los pacientes recuperados del coronavirus, y de la eventual distribución del producto.
Las dos compañías esperan obtener la aprobación de la Administración de Alimentos y Drogas de los Estados Unidos (FDA), así como de otros organismos reguladores en todo el mundo. Ambas compañías también han formado asociaciones con otras instituciones para investigar y probar sus nuevas terapias. En julio, Kedrion se asoció con el Centro Médico Irving de la Universidad de Columbia para probar una nueva terapia de inmunoglobulina (IgG) para los pacientes con coronavirus. El director médico de los laboratorios clínicos del centro, el Dr. Steven Spitalnik, afirmó en ese momento que si recibe la aprobación de la FDA, espera que pueda ser administrada a los trabajadores médicos de primera línea como medida preventiva.
Kamada está actualmente asociado con el Centro Médico de la Universidad de Hadassah, en Jerusalén, donde está probando su tratamiento de IgG bajo los auspicios del Ministerio de Salud.
El tratamiento funciona como una vacuna pasiva, que es cuando se le administran anticuerpos formados por otro paciente que contrajo la enfermedad y los desarrolló. Esto contrasta con una vacuna activa, cuando se le inyecta una versión muerta o debilitada de un virus que engaña a su sistema inmunológico haciéndole creer que ha tenido la enfermedad, y su sistema inmunológico crea anticuerpos para protegerle.
La FDA dio una “autorización de uso de emergencia” para los tratamientos contra el coronavirus que utilizan plasma sanguíneo de pacientes recuperados. El Ministerio de Salud de Israel aún no lo ha hecho, pero el jefe de Hadassah, Zeev Rotstein, les insta a seguir los pasos de la FDA.
“Desde el primer momento en que la COVID-19 atacó a Israel nos dimos cuenta de que el plasma era una herramienta importante para tratar a los pacientes enfermos”, señaló Rotstein al Jerusalén Post.
“El Ministerio de Salud se mostró reacio incluso a vernos recoger el plasma. Pero al final, los frutos son muy satisfactorios”.